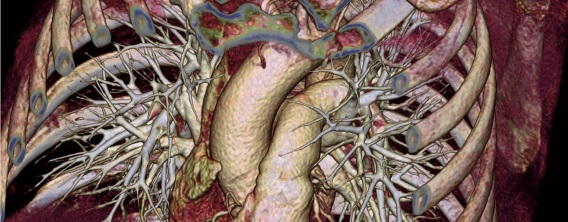
RöKo Digital – Sicherer Einsatz iodhaltiger Kontrastmittel
Aktuelle Studien relativieren das Risiko iodhaltiger Kontrastmittel. Die neuen Erkenntnisse sind teilweise bereits in die aktuellen ESUR-Leitlinien für Kontrastmittel eingeflossen.
-
Präsentationstag:21.05.2020 3 Kommentare
-
Autor:kf/ktg
-
Sprecher:Michael Uder, Universitätsklinikum Erlangen
-
Quelle:Röntgenkongress Digital 2020
„Wir dürfen eine Wahrheit nie vergessen: iodhaltige Kontrastmittel sind sehr, sehr, sehr gut verträglich“, betonte Michael Uder vom Universitätsklinikum Erlangen.
Eine weitere wichtige Wahrheit sei: Steigt das Kreatinin, und zwar egal in welchem Ausmaß, nehmen Morbidität und Mortalität zu. Uder zeigte eine ältere Studie, in der die Letalität der Teilnehmenden mit Nierenversagen (183/16.248) fünfmal höher lag (34% vs. 7%) als in der Gruppe ohne akutes Nierenversagen (Levy 1996).
Aktuelle ESUR-Leitlinien für Kontrastmittel (V 10.0)
„Hier gab es drastische Veränderungen“, so Uder.
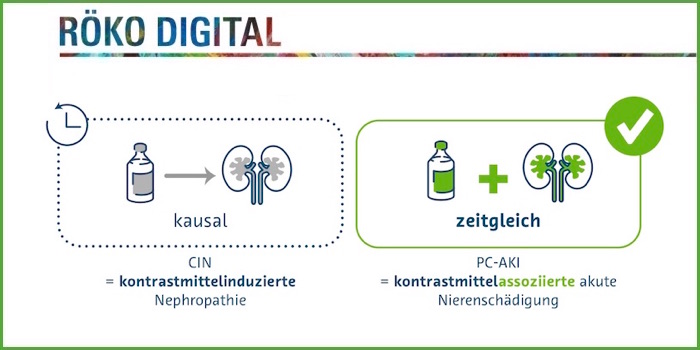
- Der Begriff „kontrastmittelinduzierte Nephropathie (CIN)“ wurde durch „kontrastmittelassoziierte akute Nierenschädigung (PC-AKI)“ ersetzt. „Damit löst man sich vom kausalen Zusammenhang zwischen möglicher Nierenschädigung und Kontrastmittelgabe.“
Grund dieser Anpassungen sind aktuelle Studienergebnisse, beispielsweise der McDonald-Gruppe: Sie ergeben ein vergleichbar hohes Risiko für akutes Nierenversagen nach nativer und kontrastmittelverstärkter CT. Dieses Ergebnis war auch nach Risikoadjustierung reproduzierbar (McDonald 2013; McDonald 2014).
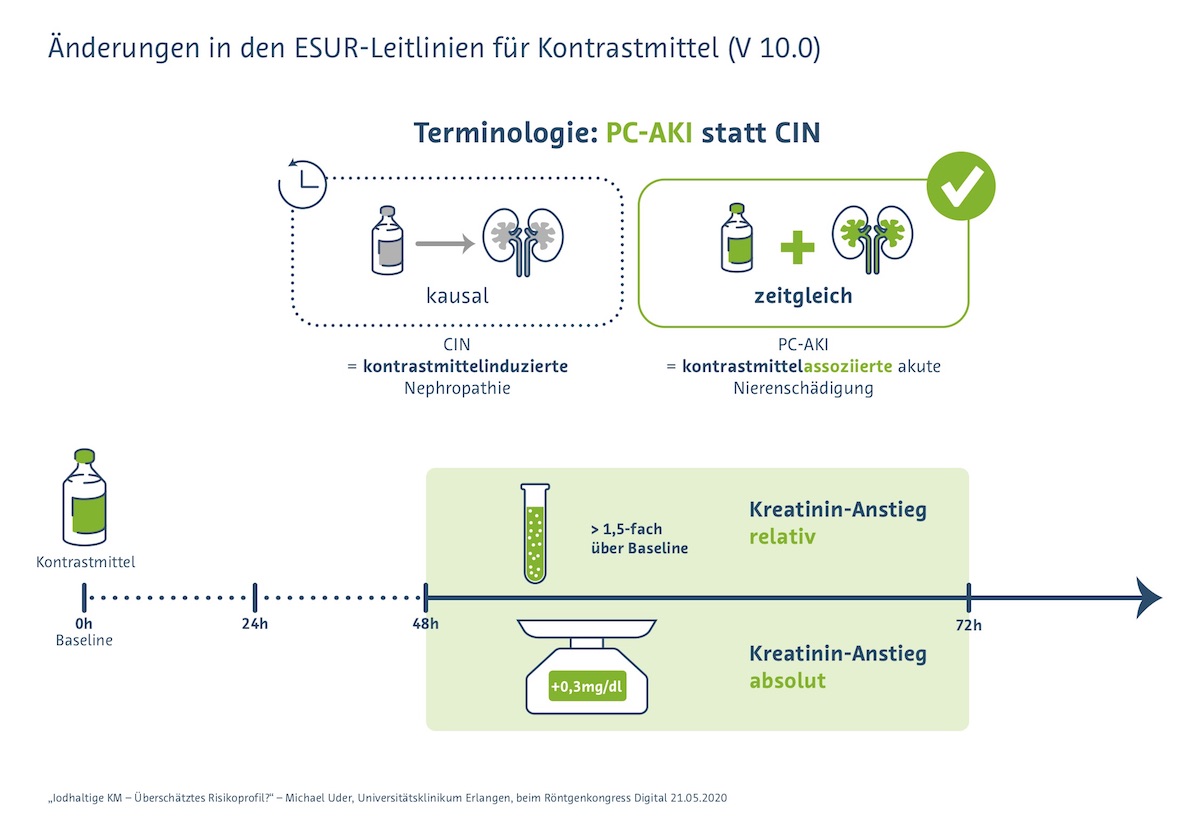
- PC-AKI wird anders definiert als bisher die CIN (= Krea-Anstieg >25% bzw. > 0,5mg/dl innerhalb von 72h nach KM).
| PC-AKI liegt vor, wenn das Kreatinin innerhalb von 48-72h nach KM-Gabe über das 1,5-Fache des Ausgangswertes bzw. um mehr als 0,3mg/dl ansteigt. |
Uder wies in diesem Zusammenhang auf die physiologischen Schwankungen des Serum-Kreatininwertes hin. So liege der Wert beispielsweise nach körperlicher Bewegung oder Stress höher als unter Ruhebedingungen. Ein physiologisch niedriger Ausgangswert kombiniert mit einem stressinduzierten Anstieg während der Untersuchung könnte als Hinweis auf eine PC-AKI fehlgedeutet werden. „Vielleicht ist das ein Grund für die angeblichen Krea-Anstiege nach nativer CT“, so Uder.
- Differenziertere Vorgaben zur protektiven i.v. Hydrierung bei:
- v. KM-Gabe und eGFR < 30ml/min/1,73m2
- a. KM-Gabe mit renaler Exposition im Second-Pass und eGFR < 30ml/min/1,73m2
- a. KM-Gabe mit renaler Exposition im First-Pass und eGFR < 45ml/min/1,73m2
Wann Kreatinin bzw. eGFR bestimmen?
Nicht vor jeder CT-Untersuchung muss das Kreatinin bekannt sein. Sinnvoll hält Uder die Bestimmung bei:
- bekannter Nierenerkrankung mit eGFR < 60ml/min/1,73m2
- nach Nieren-OP
- Proteinurie, Hypertonie oder Hyperurikämie
- DiabetikerInnen
„Der Kreatininwert darf auch etwas älter sein“, ergänzte Uder. Lediglich bei akuten Erkrankungen oder akuter Verschlechterung einer chronischen Krankheit sowie stationären PatientInnen sollte die Bestimmung nicht länger als eine Woche zurückliegen. „Bei allen anderen Patienten reicht ein Wert aus den letzten drei Monaten.“
Häufig werde er gefragt, ab welchem Kreatininwert eine KM-Gabe kontraindiziert sei. „Wenn die Indikation zwingend ist, gibt es für mich keinen Grenzwert“, so Uder.
Kritischer Blick auf die i.v. Hydrierung
Nijssen et al. haben keine Unterlegenheit für eine fehlende i.v. Hydrierung von RisikopatientInnen nachweisen können (Nijssen 2017). Uder räumte aber ein, dass die Studie nur PatientInnen mit einer eGFR von 30-59ml/min/1,73m2 einschloss.
Eine Hydrierung nach intravenöser KM-Gabe empfehlen die ESUR-Leitlinien für Kontrastmittel nur noch bei einer eGFR < 30ml/min/1,73m2. „Das kommt selten vor“, kommentierte Uder. Zudem scheint der protektive Effekt auch hier fraglich. So fand eine aktuelle Studie bei hydrierten und nicht-hydrierten PatientInnen keinen signifikanten Unterschied bei den Kreatinin-Anstiegen (Nijssen 2019). „Dafür hat die Studie gezeigt, dass Hydrierung auch gravierende Nachteile haben kann“, so Uder. In 6,7% der Fälle löste sie eine Herzinsuffizienz oder Arrhythmie aus.
Uder hielt die ESUR-Empfehlungen zur Hydrierung für „zu kompliziert“ und nannte als praktikable Alternative 100ml NaCl/h für 4h vor bis 4h nach KM-Gabe bei:
- CT oder Becken-Bein-Angiographie und eGFR < 30ml/min/1,73m2
- Koronar- oder Aorten-Angiographie und eGFR < 45ml/min/1,73m2
Zudem fehle ihm bei der Leitlinie die Rationale, warum nicht auch oral hydriert werden könne. Für Uder spricht nichts gegen eine orale Flüssigkeitszufuhr. Er nannte 1l/12h vor und 1l/12h nach KM-Gabe als Alternative „in der Not“, kombiniert mit einer i.v. Hydrierung während der Untersuchung.
Seine Aussage „Ich möchte ein wenig warnen: Vielleicht führt Hydrierung auch nur zu einer Kreatinin-Kosmetik“, bezeichnete der Referent als ‚Uder’sche Spekulation’. Dazu zeigte er eine fiktive Abbildung, in der die ‚Verwässerung‘ das Kreatinin weniger ansteigen lässt, als es in Wahrheit der Fall ist.
Unerwünschte KM-Wirkungen
Bei den akuten unerwünschten Wirkungen nach KM-Gabe wird zwischen allergieartigen (allergoiden) und chemotoxischen Reaktionen unterschieden. Die genauen Pathomechanismen beider Reaktionstypen sind bisher nicht bekannt.
Übelkeit, Erbrechen und Wärme-/Kältegefühl aber auch zerebraler Krampfanfall zählen zu den dosisabhängigen chemotoxischen Reaktionen.
Beispiele für allergoide Reaktionen sind: Urtikaria, Juckreiz, Erythem, Bronchospasmus sowie Atem- und Herzstillstand.
Akute unerwünschte Reaktionen treten vorwiegend innerhalb von wenigen Minuten nach KM-Gabe auf.
Ist anamnestisch eine frühere KM-Reaktion bekannt, empfehlen die ESUR-Leitlinien ein alternatives diagnostisches Verfahren oder ein anderes Kontrastmittel. Mit der Wahl eines anderen Kontrastmittels lässt sich das Risiko senken. In einer Studie betrug das Risiko unerwünschter Wirkungen nach erneuter Gabe des gleichen Kontrastmittels 31%, bei Substanz-Wechsel nur 12%. Die zusätzliche Gabe eines H1-Blockers reduzierte in beiden Gruppen das Risiko weiter, auf 24% bzw. 8% (Park 2018).
Zur Risikoreduktion werde in den USA noch Kortison empfohlen, sei aber sehr umstritten, sagte Uder: „Wenn Sie das machen, reicht die Gabe fünf Stunden vorher.“
Diskussion
Würden Sie Dialyse-Patienten eher iod- oder gadoliniumhaltige Kontrastmittel geben?
Uder: Ich denke, das ist egal. Elektive Untersuchungen sollten an einem geplanten Dialysetag stattfinden, dann ist das für die Patienten kein zusätzlicher Aufwand. Bei präterminaler Niereninsuffizienz muss nicht dialysiert werden. Das wäre zumindest bei iodhaltigen Röntgen-Kontrastmitteln eher von Nachteil. Zudem stimmt es auch nicht, dass Kontrastmittel die Restausscheidung verringern.
Wie schätzen Sie das Risiko durch Metformin ein?
Uder: Darüber ärgere ich mich immer, denn das Ketoazidose-Risiko konnten Studien bisher nicht ausreichend nachweisen. Da die Warnung aber im Beipackzettel steht, halten wir uns bei elektiven Indikationen daran und setzen Metformin bei einer eGFR unter 60 ml/min/1,73m² 48 Stunden vor der intravasalen Kontrastmittelgabe ab. Im Beipackzettel von Metformin steht auch, dass es bei schwerer Niereninsuffizienz (< 30 ml/min/1,73m²) kontraindiziert ist. Mit diesem Problem dürften wir also gar nicht konfrontiert sein.
Haben Sie bei Interventionen eine Kontrastmittel-Obergrenze?
Uder: Nein, wenn die Intervention indiziert ist, geben wir so viel Kontrastmittel wie nötig. Mit einer Ausnahme: Bei ganz kleinen Kindern sind wir zurückhaltend.
Wie gehen Sie mit nephrotoxischen Medikamenten um? Wie alt darf der Kreatinin-Wert sein?
Uder: Unser Ziel ist es, so viele dieser Medikamente wegzulassen wie nur möglich. Wann das Kreatinin bestimmt wurde, spielt dabei eine untergeordnete Rolle. Ist die Untersuchung indiziert, hält uns ein älterer Wert nicht davon ab.Quellen zu "RöKo Digital – Sicherer Einsatz iodhaltiger Kontrastmittel"
Levy EM, Viscoli CM, Horwitz RI.
The Effect of Acute Renal Failure on Mortality. A Cohort Analysis.
JAMA. 1996;275(19):1489-94
McDonald RJ et al.
Intravenous Contrast Material Exposure Is Not an Independent Risk Factor for Dialysis or Mortality.
Radiology. 2014;273(3):714-25
McDonald RJ et al.
Intravenous Contrast Material–Induced Nephropathy: Causal or Coincident Phenomenon?
Radiology. 2013; 267(1):106-18
Nijssen EC et al.
Prophylactic Hydration to Protect Renal Function From Intravascular Iodinated Contrast Material in Patients at High Risk of Contrast-Induced Nephropathy (AMACING): A Prospective, Randomised, Phase 3, Controlled, Open-Label, Non-Inferiority Trial.
Lancet. 2017;389(10076):1312-22
Nijssen EC et al.
Prophylaxis in High-Risk Patients With eGFR < 30 mL/min/1.73 m2: Get the Balance Right.
Invest Radiol. 2019;54(9):580-8
Park SJ at al.
Immediate Mild Reactions to CT With Iodinated Contrast Media: Strategy of Contrast Media Readministration Without Corticosteroids.
Radiology. 2018;288(3):710-6