ECR 2023 – KI-gestützte Brust-MRT

Die rasante Entwicklung der Künstlichen Intelligenz verändert auch die Brustbildgebung.
-
Präsentationstag:01.03.2023 0 Kommentare
-
Autor:kf/ktg
-
Sprecher:Katja Pinker-Domenig, Sloan Kettering Memorial Center, New York
-
Quelle:ECR 2023
| Künstliche Intelligenz bietet "noch nie dagewesene Chancen", den klinischen Nutzen der Bildgebung zu steigern. Allerdings sind noch technische, rechtliche und ethische Probleme zu lösen. |
„Breite“ und „enge“ Künstliche Intelligenz
Katja Pinker-Domenig, Sloan Kettering Memorial Center, New York, unterteilt KI-Anwendungen in der Bildgebung in zwei grundlegende Kategorien (Hickman 2021):
- “Breite” (broad) KI, die für organisatorische oder administrative Zwecke eingesetzt wird, beispielsweise für repetitive oder routinemäßige Aufgaben wie Kontrastadjustierung oder Qualitätssicherung der Scans. Ein praktisches Beispiel für breite KI ist die diffusionsgewichtete Bildgebung (DWI) mit Deep Learning (DL) Rekonstruktion: Letztere kann die DWI von vier auf zwei Minuten halbieren.
- “Enge” (narrow) KI lässt sich als Unterstützung für Kliniker:innen oder autark einsetzen. Ziel dieser KI-Lösungen ist, den Outcome für Patient:innen und die Effizienz im Gesundheitssystem zu verbessern. Enge KI umfasst die computergestützte Erkennung von Läsionen, sowie Diagnose und Triage, aber auch Läsionssegmentierung, das Einschätzen der Wahrscheinlichkeit des Therapieansprechens und die Risikovorhersage.
Pinker-Domenig hält die enge KI aufgrund ihrer direkten klinischen Auswirkungen für die interessantere der beiden genannten. Sie stellte ein breites Spektrum aktueller Studien vor, die die Einsatzmöglichkeiten der engen KI für die Brust-MRT aufzeigen.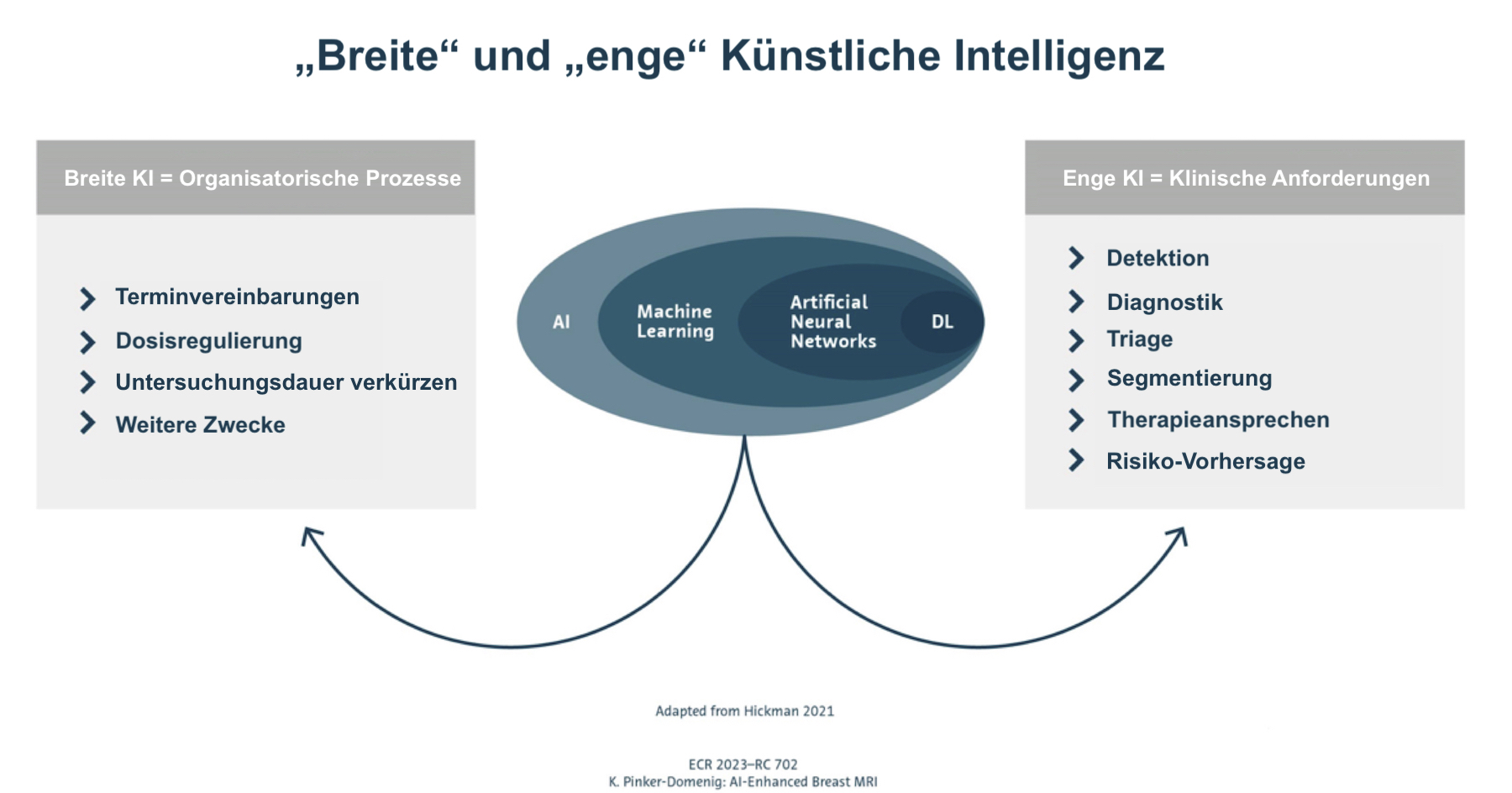
Anwendung: Triage
Eine Sekundäranalyse der DENSE-Studiendaten untersuchte die Nutzbarbarkeit eines automatisierten Deep-Learning-Modells für die Screening-Triage (Verburg 2022) bei Frauen mit dichtem Brustgewebe. Das DL-Modell differenzierte zwischen Mammae mit und ohne Läsionen. Die Studie zielte darauf ab, möglichst viele MRT-Untersuchungen ohne Läsionen auszusortieren, gleichzeitig aber karzinomverdächtige Läsionen richtig zu identifizieren. Bei der automatisierten Analyse der Mamma-MRTs wurden 40 % der MRT-Untersuchungen ohne Läsionen aussortiert, ohne dass Karzinome übersehen wurden. Dies bedeutet, dass das KI-Modell bei gleichbleibender Qualität den Zeitaufwand für das Screening-Programm verkürzt.
Anwendung: Screening
Eine Studie der Universität Groningen, Niederlande (Jing 2022), zeigte, dass ein DL-Modell in der ultraschnellen Brust-MRT Normalbefunde automatisch identifizieren kann. So ließe sich die Arbeitsbelastung der Radiolog:innen und die Scan-Zeit reduzieren.
Eine weitere Studie aus Pinker-Domenigs Institution überprüfte, ob DL die Schichten eines Scans erkennt, die potenzielles Tumorgewebe abbilden (Eskreis-Winkler 2021). Die diagnostische Genauigkeit der Erkennung dieser Slices betrug 92,8%, die Sensitivität 89,5% und die Spezifität 94,3%. Die DL konnte also tumorverdächtige Schichten mit hoher Genauigkeit identifizieren. Ohne Deep-Learning-Algorithmus benötigten die Befunder:innen 3 bis 45 Sekunden, um zu den tumorverdächtigen Slices zu scrollen. Dieses Scrollen ließe sich durch die Integration dieses Modells ins PACS umgehen. Das Modell kann auch die Suche bei unsystematischer Bildbetrachtung erleichtern, zum Beispiel In interdisziplinären Tumor-Konferenzen.
Anwendung: Klassifizierung
Eine Studie des Radboud University Medical Center, Nijmegen, Niederlande, untersuchte die KI-basierte Klassifizierung benigner und maligner Mammaläsionen, die mit multiparametrischer MRT gescannt wurden, einschließlich ultraschneller dynamischer kontrastverstärkter (DCE) MRT, T2w und DWI (Dalmis 2019).
DL-Methoden wurden zur Befundung der ultraschnellen DCE-MRI- und T2w-Bilder verwendet. Zur endgültigen Charakterisierung der Läsion kombinierte ein Random-Forest-Klassifikator die Ergebnisse mit Patientinnen-Daten und dem ADC (Apparent Diffusion Coefficient). Die Ergebnisse wurden mit der prospektiven Befundung durch Radiolog:innen verglichen. Die Ergebnisse waren ähnlich, aber die KI reduzierte die Falsch-Positiven. Die Autor:innen folgern, dass die KI-Befundung die Spezifität der multiparametrischen ultraschnellen MRT verbessert.
Um die diagnostische Leistungsfähigkeit verschiedener Methoden bei der Klassifizierung kontrastverstärkter Mamma-Läsionen einzuschätzen, verglich eine Studie der Universität Aachen die Radiomics-Analyse (RA) mit der Befundung durch ein Convolutional Neural Network (CNN) und der Befundung durch Radiolog:innen (Truhn 2019). CNN war RA bei der Klassifizierung kontrastverstärkter Läsionen als gut- oder bösartig zwar überlegen, allerdings waren beide Ansätze der Klassifizierung der Radiolog:innen unterlegen. Mehr Trainingsdaten können die CNN-Leistung verbessern, nicht aber die Leistung der RA. Pinker-Domenigs Kommentar: "Radiologen werden in absehbarer Zeit nicht arbeitslos sein.“
Eine weitere, multizentrische retrospektive Studie beschäftigte sich mit der Erkennung von Mammakarzinomen durch RA kombiniert mit maschinellem Lernen (ML). Sie nutzte dazu die multiparametrische MRT mit DCE- und DWI-Radiomics-Modellen separat und kombiniert (Daimiel Naranjo 2021). Es zeigte sich, dass RA in Verbindung mit ML die Bewertung verdächtiger, kontrastanreichender Mammatumoren verbessert, für die normalerweise eine Biopsie empfohlen wird. Das RA-ML-Modell spezifiziert die Diagnose und reduziert somit die Anzahl unnötiger Biopsien. Der Einsatz des Modells führte auch dazu, dass Fälle mit initialer Biopsieempfehlung auf die Handlungsempfehlung „Nachuntersuchung“ zurückgestuft werden konnten, ohne dass Karzinome übersehen worden wären, betonte Pinker-Domenig.
In einer weiteren Studie aus Pinker-Domenigs Institution wurde untersucht, ob RA plus ML unnötige Biopsien bei BRCA-positiven Patientinnen mit kleinen Mass-Lesions unter einem Zentimeter vermeiden hilft (Lo Gullo 2020). Kleine Mass-Lesions sind erstens schwer zu charakterisieren, und zweitens helfen auch die BIRADS-Deskriptoren bei BRCA+-Patientinnen hier nicht weiter. RA plus ML verbesserte die diagnostische Genauigkeit der MRT bei der Charakterisierung dieser Läsionen im Vergleich zur qualitativen morphologischen Beurteilung durch zwei Radiolog:innen, die die BI-RADS-Klassifikation verwendeten. Das Modell könnte also nicht nur zu besserer Diagnostik führen, sondern vor allem wenig erfahrene Radiolog:innen unterstützen.KI-unterstütze PET/MRI: Klassifizierung
Für die multiparametrische 18F-FDG-PET/MRT ergibt eine aktuelle Studie, dass ein Radiomics-ML-Modell mit quantitativen Parametern und Radiomics-Features maligne und benigne Mamma-Läsionen mit hoher diagnostischer Genauigkeit unterscheiden kann (Romeo 2021). Die KI ist in der Lage, Informationen aus verschiedenen Modalitäten zusammenzuführen.
Anwendung: Unterscheidung molekularer Subtypen mit DCE
Das Differenzieren molekularer Subtypen ist derzeit noch nicht in der klinischen Anwendung. "Es könnte noch einige Zeit dauern, die klinischen Kollegen davon zu überzeugen“, so Pinker-Domenig. Dennoch zeigen verschiedene präliminäre Studien den potenziellen Nutzen der Methode. Pinker-Domenig griff ein Beispiel heraus (Leithner 2019): Die Auswertung bestimmter Radiomics-Signaturen, die aus der kontrastverstärkten MRI extrahiert wurden, zeigte eine hohe diagnostische Genauigkeit für die Beurteilung des Rezeptorstatus und der molekularen Subtypen von Mammakarzinomen. Die Ergebnisse müssen jedoch noch in größeren Studien bestätigt werden. Die Differenzierung molekularer Subtypen ist auch mit DWI möglich.
Anwendung: MR-Phänotypen und Tumor-Genexpression
Eine weitere Studie widmete sich dem Zusammenhang zwischen MRT-Phänotypen von Mammakarzinomen und der ihnen zugrunde liegenden Molekularbiologie (Bismeijer 2020). Computergenerierte MR-Merkmale wurden mit der Genexpression verglichen. Die für die Gen-Sequenzierung nötige Tumor-RNA stammte aus dem histologischen Präparat der Karzinome. Es zeigte sich, dass die MRT-Merkmale „Kontrastverstärkung“ und „scharfe Tumorberandung“ mit der Expression ribosomaler Proteine korrelieren.
Diese Ergebnisse legen nahe, dass diese beiden MRT-Merkmale als „Bildgebungs-Biomarker“ für Medikamente fungieren könnten, die auf das Ribosom abzielen. Die Radiologie könnte also zu einer gezielteren Behandlung beitragen.Anwendung: Therapieansprechen
Ein ML-Modell mit klinischen und radiologischen MRT-Merkmalen kann bei HER2-überexprimierenden Mammakarzinom-Patientinnen das HER2-Expressionsniveau quantifizieren und außerdem die pathologische Komplettremission (pCR) nach neoadjuvanter Chemotherapie (NAC) vorhersagen (Bitencourt 2020). pCR gilt als Maßstab für den Erfolg der NAC und als Surrogatparameter für das Risiko eines erneuten Auftretens und das Langzeitüberleben.
Auch die Radiomics-Signatur aus der multiparametrischen MRT könnte ein potenzielles Instrument für die Vorhersage der pCR auf NAC bei Brustkrebs vor Beginn der Behandlung werden (Liu 2019).
Eine andere Studie untersuchte ein multimodales Deep-Learning-Modell, das klinische Informationen und MR-Bilder vor der Behandlung kombiniert, um die pCR nach NAC bei Patientinnen mit Mammakarzinom (Joo 2021) zu prognostizieren. Auch dieses Modell war in der Lage, das Ansprechen auf eine Chemotherapie vorherzusagen. Ansätze zur Entwicklung eines klinisch nutzbaren Tools – basierend auf einem Transfer-Learning-Ansatz – für eine frühzeitige Vorhersage der pCR auf NAC sind bereits im Gange (Comes 2021).
Auch durch eine 18F-FDG-PET/MRT-Radiomics-Analyse lässt sich die pCR vor der NAC vorhersagen, insbesondere bei hormonrezeptorpositiven, aber HER2-negativen Patientinnen (Umutlu 2022). Die 18F-FDG-PET/MRT ermöglicht einen individualisierten und gezielten Behandlungsansatz und die Patientinnenstratifizierung vor Therapiebeginn.Anwendung: Rezidiv-Scores mit DCE-MRT
Oncotype Dx ist eine leistungsfähige, aber invasive und teure genetische Analyse, die einen Rezidiv-Score (RS) liefert. Sie sagt quantitativ den Outcome bei nodalnegativen Patientinnen mit invasivem Mammakarzinom und ER+ /HER2- Rezeptorstatus voraus. Die aktuelle Deep-CNN-Architektur lässt sich auch für Oncotype DX RS trainieren – das heißt, sie kann das Rezidivrisiko prognostizieren (Ha 2019) und könnte möglicherweise sogar Oncotype Dx ersetzen. Eine große Multikohortenstudie stützt diese Ergebnisse. Ein Modell, das den Rezidiv-Score mit weiteren, komplementären Merkmalen kombiniert, konnte das Ansprechen auf NAC (Fan 2022) bei Patientinnen mit ER+ Brustkrebs noch genauer vorhersagen.
Anwendung: Risikobewertung
Nächste Schritte
Die Studien zeigen, dass so genannte enge KI die klinische Versorgung verbessern kann. Patientinnen scheinen KI generell zu akzeptieren. "Die größte Herausforderung wird darin bestehen, sie in die Klinik zu bringen – man denke nur daran, wie lange es gedauert hat die MRT einzuführen“, kommentierte Pinker-Domenig. Alle Referent:innen waren sich einig, dass die Schaffung der juristischen Rahmenbedingungen einer der wichtigsten nächsten Schritte ist. Mit anderen Worten: Die Beteiligten müssen herausfinden, wie ein Computer verklagt werden kann.
Referenzen "ECR 2023 – KI-gestützte Brust-MRT"
Bismeijer T et al. Radiogenomic Analysis of Breast Cancer by Linking MRI Phenotypes with Tumor Gene Expression. Radiology 2020;296(2):277-87
https://doi.org/10.1148/radiol.2020191453
Bitencourt AGV et al. MRI-based machine learning radiomics can predict HER2 expression level and pathologic response after neoadjuvant therapy in HER2 overexpressing breast cancer. EBioMedicine 2020;61:103042
https://doi.org/10.1016/j.ebiom.2020.103042
Comes MC et al. Early prediction of neoadjuvant chemotherapy response by exploiting a transfer learning approach on breast DCE-MRIs, Sci Rep. 2021;11(1):14123
https://doi.org/10.1038/s41598-021-93592-z
Daimiel Naranjo I et al. Radiomics and Machine Learning with Multiparametric Breast MRI for Improved Diagnostic Accuracy in Breast Cancer Diagnosis. Diagnostics (Basel) 2021;11(6):919
https://doi.org/10.3390/diagnostics11060919
Dalmis MU et al. Artificial Intelligence-Based Classification of Breast Lesions Imaged With a Multiparametric Breast MRI Protocol With Ultrafast DCE-MRI, T2, and DWI. Invest Radiol 2019;54(6):325-32
https://doi.org/10.1097/RLI.0000000000000544
Eskreis-Winkler S et al. Using Deep Learning to Improve Nonsystematic Viewing of Breast Cancer on MRI. Journal of Breast Imaging 2021;3(2): 201–7
https://doi.org/10.1093/jbi/wbaa102
Fan M et al. Radiogenomic Signatures of Oncotype DX Recurrence Score Enable Prediction of Survival in Estrogen Receptor-Positive Breast Cancer: A Multicohort Study. Radiology 2022;302(3):516-24
https://doi.org/10.1148/radiol.2021210738
Ha R et al. Convolutional Neural Network Using a Breast MRI Tumor Dataset Can Predict Oncotype Dx Recurrence Score. JMRI 2019; 49(2):518-24
https://doi.org/10.1002/jmri.26244
Hickman SE et al. Adoption of artificial intelligence in breast imaging: evaluation, ethical constraints and limitations. British Journal of Cancer 2021;125:15–22 https://doi.org/10.1038/s41416-021-01333-w
Jing X et al. Using deep learning to safely exclude lesions with only ultrafast breast MRI to shorten acquisition and reading time. Eur Radiol 2022;32:8706–15
https://doi.org/10.1007/s00330-022-08863-8
Joo S et al. Multimodal deep learning models for the prediction of pathologic response to neoadjuvant chemotherapy in breast cancer. Sci Rep 2021 Sep 22;11(1):18800.
https://doi.org/10.1038/s41598-021-98408-8
Leithner D et al. Radiomic signatures with contrast-enhanced magnetic resonance imaging for the assessment of breast cancer receptor status and molecular subtypes: initial results. Brest Cancer Res 2019:21(1):106
https://doi.org/10.1186/s13058-019-1187-z
Lui Z et al. Radiomics of Multiparametric MRI for Pretreatment Prediction of Pathologic Complete Response to Neoadjuvant Chemotherapy in Breast Cancer: A Multicenter Study. Clin Cancer Res 2019;25(12):3538-47
https://doi.org/10.1158/1078-0432.CCR-18-3190
Lo Gullo R et al. Improved characterization of sub-centimeter enhancing breast masses on MRI with radiomics and machine learning in BRCA mutation carriers. Eur Radiol 2020;30(12):6721-31
https://doi.org/10.1007/s00330-020-06991-7
Portnoi T et al. Deep Learning Model to Assess Cancer Risk on the Basis of a Breast MR Image Alone. AJR Am J Roentgenol 2019;213(1):227-33
https://doi.org/10.2214/AJR.18.20813
Romeo V et al. AI-enhanced simultaneous multiparametric 18F-FDG PET/MRI for accurate breast cancer diagnosis. Eur J Nucl Med Mol Imaging 2022;49(2):596-608
https://doi.org/10.1007/s00259-021-05492-z
Truhn D et al. Radiomic versus Convolutional Neural Networks Analysis for Classification of Contrast-enhancing Lesions at Multiparametric Breast MRI. Radiology 2019;290(2):290-297
https://doi.org/10.1148/radiol.2018181352
Umutlu L et al. Multiparametric 18F-FDG PET/MRI-Based Radiomics for Prediction of Pathological Complete Response to Neoadjuvant Chemotherapy in Breast Cancer. Cancers 2022, 14(7), 1727
https://doi.org/10.3390/cancers14071727
Verburg E et al. Deep Learning for Automated Triaging of 4581 Breast MRI Examinations from the DENSE Trial. Radiology 2022;302(1):29-36
https://doi.org/10.1148/radiol.2021203960