RöKo 2021 – KI-Tools für die Lunge

Zahlreiche KI-basierte Tools für die Lungendiagnostik sind zwar zugelassen, besitzen aber noch nicht das nötige Vertrauen. Für das zügige Validieren von Algorithmen ist die Zusammenarbeit über die Grenzen von Institutionen und Ländern hinweg unerlässlich.
-
Präsentationstag:17.04.2021 0 Kommentare
-
Autor:mh/ktg
-
Sprecher:Horst Hahn, Fraunhofer MEVIS Bremen
-
Quelle:RöKo 2021
Horst Hahn von Fraunhofer MEVIS, Bremen, diskutierte beim RöKo 2021 aktuelle Einsatzbereiche für KI-basierte Tools zur Lungendiagnostik.
KI-Tools für aufwendige Arbeiten
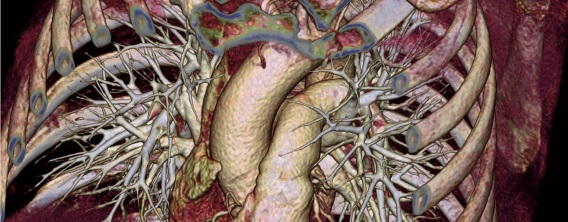
Für die Diagnostik pulmonaler Gefäßerkrankungen ist die Trennung von Arterien und Venen relevant. Diese Trennung manuell anhand von CT-Aufnahmen des Thorax vorzunehmen ist aufwendig und im klinischen Alltag kaum machbar.
Dass die automatische Trennung von Arterien und Venen mittels eines 3D Convolutional Neural Network (CNN) gelingt, zeigten Nardelli P et al. (IEEE Trans Med Imaging 2018). Ihr Algorithmus erzielte eine Genauigkeit von 94%.
KI beschleunigt Entwicklung von Algorithmen
Die Lungenlappensegmentierung spielt in der klinischen Praxis eine wichtige Rolle und ist besonders bei schweren Erkrankungen und inkompletten interlobären Fissuren herausfordernd. Für die aufwendige Entwicklung ihres 2012 veröffentlichten Algorithmus’ zur automatischen Lungenlappensegmentierung benötigten Lassen B et al. (IEEE Trans Med Imaging 2013) rund zwei Jahre. Acht Jahre später entwickelten dieselbe Autorin und Team in nur zwei Wochen „und mit relativ wenig Datensätzen“, wie Hahn betonte, einen U-Net-basierten Ansatz (MIDL 2020 Conference) für die automatische Segmentierung der Lungenlappen.
Für die Diagnostik von CoViD-19 wurden in kürzester Zeit Algorithmen entwickelt. Sie dienen der Klassifikation, der Differentialdiagnostik, dem Staging und der Beurteilung von Komorbiditäten. Letzteres sei eine „sehr wertstiftende Anwendung von KI-Tools“, so Hahn, weil weitere Aspekte der thorakalen Bildgebung aus Zeitgründen oft nicht befundet würden.
Daten lokal belassen, Algorithmen lokal anwenden
Um – gerade im Zusammenhang mit CoViD-19 – KI-Tools möglichst schnell zu validieren, ist institutionsübergreifende und internationale Zusammenarbeit erforderlich. In Deutschland haben sich im Netzwerk RACOON (Radiological Cooperative Network zur Covid-19 Pandemie) alle Universitätskliniken zusammengeschlossen. Einer der technischen Partner ist Fraunhofer MEVIS. „Die Universitätsklinika gehen mit RACOON zwar in Vorleistung, aber grundsätzlich ist das Netzwerk auch für andere Krankenhäuser offen“, betonte Hahn.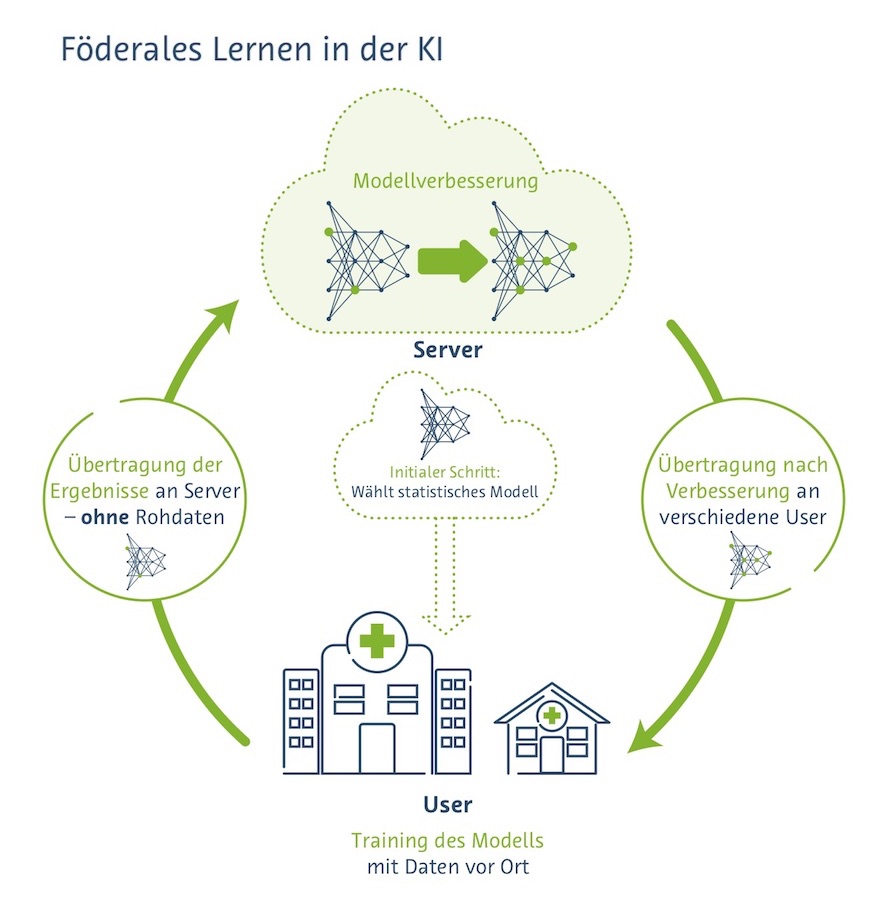
Es geht darum, Schnittstellen zu öffnen, die KI-Tools für die lokale Anwendung auszuliefern und sie lokal anzuwenden. Die sensiblen patientInnenbezogenen Daten bleiben dabei ausschließlich auf den Servern der Kliniken. „Das wird in Zukunft immer wichtiger werden“, so Hahn. Der Gesamtdatensatz bleibt damit verteilt auf unterschiedliche Institutionen. Dieser Ansatz wird als „Federated Learning“ bezeichnet.
45 Thorax-Algorithmen bei grand-challenge.org
Identische Algorithmen an vielen unterschiedlichen Standorten einsetzen – das ist auch ein Ansatz von grand-challenge.org. Unter dem Label „AI for Radiology“ bietet die Plattform eine umfangreiche Liste KI-basierter Software für die Radiologie. Von den derzeit 156 für die EU zertifizierten Produkten befassen sich 45 mit der Thorax-Bildgebung.
Neue KI-Tools zügig validieren
„Wir brauchen die Zusammenarbeit aller, also von Technik und Medizin, um nicht nur viele einzelne Inseln entstehen zu lassen, sondern um schnell herauszuarbeiten, welches die wirklich wichtigen Anwendungen sind“, plädierte Hahn für ein zügiges Validieren der vielen neuen Methoden. Derzeit gebe es eine Reihe von Produkten, die zwar schon zugelassen sind, aber noch nicht das nötige Vertrauen bei den potentiellen Anwendern genießen.
Referenzen
Lassen B et al. Automatic segmentation of the pulmonary lobes from chest CT scans based on fissures, vessels, and bronchi
IEEE Trans Med Imaging 2013;32(2):210-22
Lassen-Schmidt B et al. Automatic segmentation of the pulmonary lobes with a 3D u-net and optimized loss function
MIDL 2020 Conference (Medical Imaging with Deep Learning)
Nardelli P et al. Pulmonary Artery-Vein Classification in CT Images Using Deep Learning
IEEE Trans Med Imaging 2018;37(11):2428-2440